IVDR (EU) 2017/746 新要求概要:
一、IVDR新要求背景
新的IVDR将于2022年5月4日起强制执行。要求最终由欧洲医疗器械电子注册系统Eudamed来实现。Eudamed包括以下电子系统:
① 器械注册电子系统
② UDI数据库
③ 经济运营商备案登记电子系统
④ 公告机构和证书电子系统
⑤ 性能研究电子系统
⑥ 警戒和上市后监管电子系统
⑦ 市场监管电子系统
该系统涉及的对应企业功能如下:
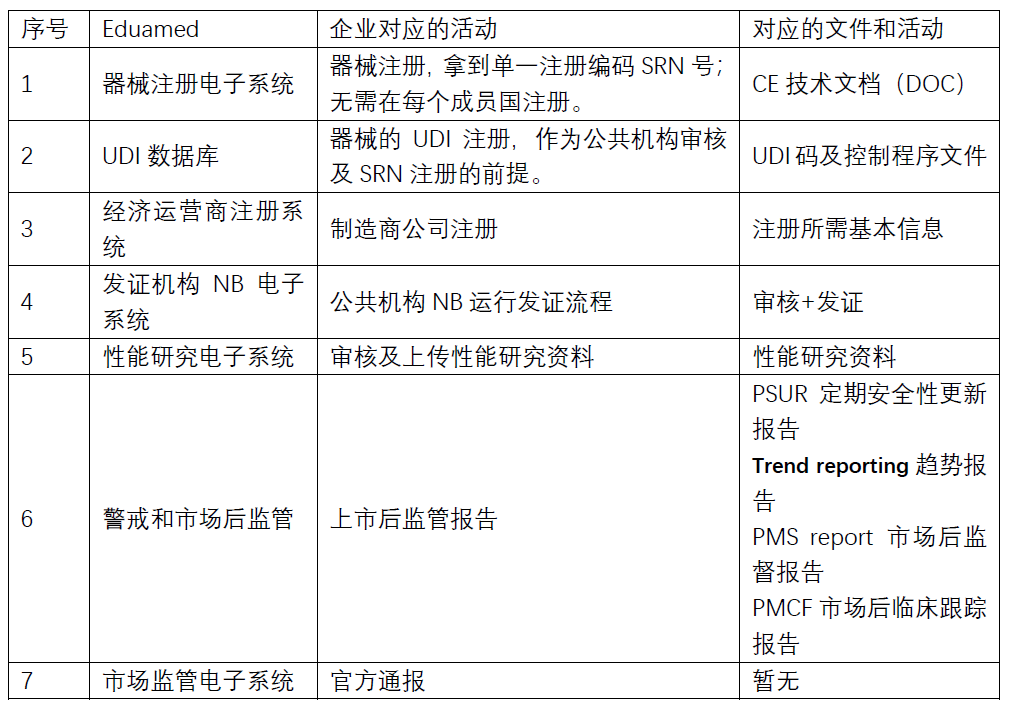
二、IVDR新要求内容
1 CE技术文档
使用国际公认的医疗器械命名
参考附录II技术文件
新涵盖UDI 编码文件
风险系统文件
性能评估和和上市后跟踪文件(PMPF)
CE技术文档A部分上报后获得单一注册号SRN
2 UDI 技术文档
DI 器械标识
PI生产标识
UDI-DI部分要提交于系统和给NB机构。上市后监管和不良事件处理都要涉及UDI。UDI在UDI数据库注册后获得注册号。UDI还要体现在自由销售证书FSC和CE自我申明DoC中。
3 企业文档
涉及企业注册各种报表填写,具体由官方数据库规定。一般来说跟CE技术文档的A部分类似。
4质量管理体系
(a) 法规符合性战略,包括符合性评估流程的遵守和系统所涵盖的器械的变更管理;
(b) 确定适用的通用安全与性能要求,寻找满足这些要求的选项;
(c) 管理责任;
(d) 资源管理,包括选择和管理供应商和分包商;
(e) 附录I第3节规定的风险管理;
(f) 性能评估,根据第56条和附录XIII的规定,包括上市后的性能追踪;
(g) 产品实现规划,包括规划、设计、研发、生产和服务提供;
(h) 根据第24(3)条为所有相关器械的UDI分配验证,并确保根据第26条提供的信息的一致性和有效性;
(i) 根据第78条的要求,建立、实施和维护上市后监管体系;
(j) 与主管机构、公告机构、其他经济运营商、客户和/或其他利益相关人沟通;
(k) 警戒情况下的严重事件和现场安全纠正措施的报告流程;
(l) 纠正措施和预防措施的管理及其有效性的验证;
(m) 产品,数据分析和产品改进的监督和评估流程。
5风险管理体系
风险评估中应包含:技术更新风险评估,现场安全纠正措施风险评估,临床效益风险评估。
有贯穿整个生命周期的风险管理体系。风险管理建立后第一年更新,随后每两年一更新。要符合持续合规。
6上市后监管体系
上市后监管计划
涵盖:
警戒系统
技术升级风险评估
现场通告,现场纠正措施
主动收集售后投诉和举报
临床风险跟踪措施,PMPF(上市后性能跟踪)
性能评估
不合格召回
7伦理审批
A,B类器械不需要到欧盟做临床性能评估,C,D类需要去欧盟做临床性能评估。
剩余样本临床性能评估计划无须欧盟审批,但需要伦理审批。需要满足《赫尔辛基宣言》。临床计划应符合ISO14155.
8研究计划
C,D类在欧盟参考实验室依据CS做性能评估(分析,诊断灵敏度等项目)是临床研究的前提。
需要提交研究计划到欧盟数据库,剩余样本研究不需要审批,但研究计划更改和变更需要审批。临床研究结束后或暂停后三个月内需要提交结果总结,研究报告。
9临床证据
包含:
性能评估(分析性能+临床性能)
科学数据(技术文件)
临床性能(需验证交叉,干扰)
PMPF(上市后性能追踪)
效益风险评估
10 PSUR(定期安全性更新报告)
C类和D类器械的制造商应编制定期安全性更新报告(“PSUR”)
PSUR应列出:
(a) 效益风险监测的结论;
(b) 上市后性能跟踪报告(PMPF)的主要结果;以及
(c) 器械的销售量和使用器械的群体规模与其他特性的评估,以及实际运行时器械的使用频率。
C类和D类器械的制造商应至少每年对PSUR进行更新。PSUR应属于附录II和III中所规定技术文件中的一部分。
C类器械制造商应向参与符合性评估的公告机构提交PSUR,并应主管机构要求向其提供报告
严重事件和现场安全纠正措施的报告和现场安全通告,以及提供定期汇总报告、上市后监管报告、定期安全性更新报告(PSUR)以及趋势报告;
11趋势报告
向相关主管机构报告以下内容:
(a) 任何涉及在欧盟市场上所提供器械的严重事件,除了在产品信息和技术文件中清楚记录并量化的预期错误结果,此类事件应根据第83条进行趋势报告
(b) 报告现场安全纠正措施、制造商提供定期汇总报告和趋势报告的时间表;
12 PMPF
上市后性能追踪(PMPF)
参见附录XIII 性能评估、性能研究和上市后跟踪(PMPF)
PMPF计划应至少包括:
(a) 应用PMPF的一般方法和流程,如收集获得的临床经验、使用者反馈、科学文献筛选和其他性能或科学数据来源;
(b) 应用PMPF的具体方法和流程(例如,环形比对试验和其他质量保证活动、流行病学研究、合适的患者评估或疾病登记、遗传数据库或上市后临床性能研究);
(c) (a)和(b)中所述的方法和流程适当性的理由;
(d) 参考本附录A部分第1.3节所所述的性能评估报告的相关部分以及附录I
第3节所述的风险管理;
(e) PMPF要解决的具体目标;
(f) 与等效或类似器械相关的性能数据评估,以及技术发展最新水平;
(g) 参考制造商使用的所有CS、协调标准和相关PMPF指南;
(h) 由制造商进行的PMPF活动的详细且充分合理的时间表(例如,PMPF数据和报告分析)。
13不良事件报告
UDI用于报告严重不良事件及现场安全纠正措施
临床性能研究生成唯一的标识号用于报告严重不良事件及现场安全纠正措施
性能研究中:申办方应充分记录以下所有情况:
(a) 在性能研究计划中发现对性能研究结果的评估至关重要的任何不良事件类型;
(b) 任何严重不良事件;
(c) 任何如未采取适当措施、未发生干预或情况不利时,可能导致严重不良事件的器械缺陷;
14 CE证书的签发
D类器械由NB审批+政府审批。D类器械实行批批签
B,C类器械由NB审核发证。
D类器械由欧盟参考实验室进行性能验证
性能验证涵盖(分析性能+安全性能)分析性能验证计划需涵盖:原理,目的,方法,检测,统计,并可执行。
B,C类器械由通告机构验证
A类企业自行验证
B类技术文件的审批参照附录IX 4.4-4.8和附录I和附录II。涵盖:CS,协调标准,性能评估,溯源,培训,PMPF,风险,警戒等。
加强质量管理体系飞行检查。
B,C类需要审核《趋势报告》
证书提交于证书系统数据库。
CE证书是准许上市和获得FSC的前提。
15 自由销售证书FSC
自由销售证书应列明器械基本UDI-DI。自由销售证书应列出公告机构签发的唯一识别号以标识此证书。自由销售证书,应制造商或授权代表要求,制造商或授权代表注册地所在成员国需签发一份自由销售证书。
16 分类规则
参考附录VIII
规则1
用于以下用途的器械归类为D类:
- 检测血液、血液成分、细胞、组织或器官,或其任何衍生物是否存在或显露传染性因子,以评估它们是否适用于输血、器官移植或细胞给药。
- 检测是否存在或显露传染性因子,其会导致危及生命的疾病,并且具有高的或可疑的传播风险。-确定危及生命的疾病的病原体载量,其监控对于患者管理的过程十分关键。
规则2
器械预期用于血型分型或组织分型,以确保用于输血或移植或细胞给药的血液、血液成分、细胞、组织或器官具有免疫相容性,此类器械归类为C类,但用于确定以下任何标记物的器械除外:
- ABO系统 [A(ABO1)、B(ABO2)、AB(ABO 3)];
- 恒河猴(Rhesus)系统 [RH1(D)、RHW1、RH2(C)、RH3(E)、RH4(C)、RH5(E)];
- KELL系统 [Kel1(K)];
- KIDD系统 [JK1(JKA)、JK2(JKB)];
- DUFFY系统 [FY1(FYA)、FY2(FYB)],
在这种情况下,它们被归为D类。
规则3
器械被归为C类,若其目的是:
(a) 用于检测是否存在或显露性传播病原体的;
(b) 用于检测是否在脑脊液或血液中存在某种高的或可疑的高传播风险的病原体;
(c) 用于检测病原体的存在,其报告结果若错误可带来引起个人、胎儿、胚胎或个体的后代死亡或严重残疾的重大风险;
(d) 用于女性的产前筛查,确定其对感染原的免疫状况;
(e) 用于确定感染性疾病的状态或免疫状态,若其报告结果将会引起患者治疗决定导致危及患者或患者后代生命的风险;
(f) 用作伴随诊断;
(g) 用于疾病分期,若其报告结果错误将会引起患者治疗决定导致危及患者或患者后代生命风险的;
(h) 用于癌症的筛查、诊断或分期;
(i) 人类基因检测;
(j) 用于检测药用产品、物质或生物组分的水平,若其报告结果错误将会引起患者治疗决定导致危及患者后代生命的风险;
(k) 对危及生命的疾病或病症患者,进行患者管理;
(l) 用于筛查胚胎或胎儿的先天性疾病;
(m) 用于新生儿的先天性疾病筛查,未能检测和治疗这些疾病可能导致危及生命的情况或严重残疾。
规则4
(a) 自测器械归为C类,但用于妊娠检测、生育力测试、确定胆固醇浓度以及检测葡萄糖、红细胞、白细胞和尿样本中细菌的器械除外,这些器械归为B类。
(b) 床旁检测器械根据其本身特性进行分类。
规则5
以下器械归为A类:
(a) 一般实验室使用的产品、没有危险特征的附件、缓冲液、洗涤液、一般培养基和组织学染色液,制造商使其适用于相关某一特定检查的体外诊断流程;
(b) 制造商专门用于体外诊断流程的器械;
(c) 样品容器。
规则6
上述分类规则未涵盖的器械归类为B类。
规则7
不具有定量或定性赋值的质控品的器械归类为B类。


 扫一扫添加微信
扫一扫添加微信